岛津GC家族全面助力中国药典0861通则修订

自2017年国家药品监督管理局(简称NMPA)正式加入国际人用药品注册技术协调会(ICH)之后,国家药典委逐步开展与ICH相关指导原则的协调研究工作。随着2025版药典发布的临近,中国药典四部通则陆续发布了重要的修改稿公示。其中,与Q3C指导原则对应的中国药典通则0861的修订内容备受关注,当前化学药、生物制品、中药等各大类药品均涉及对残留溶剂的控制与分析。2023年11月21日,国家药典委发布0861标准草案修订公示稿(第一次),通过对比原0861与ICH Q3C、欧洲药典5.4、美国药典467以及日本药局方2.46残留溶剂的异同,在协调的基础上进行了修订。
参考起草说明,津津老师对通则0861修订的主要情况进行了如下整理:
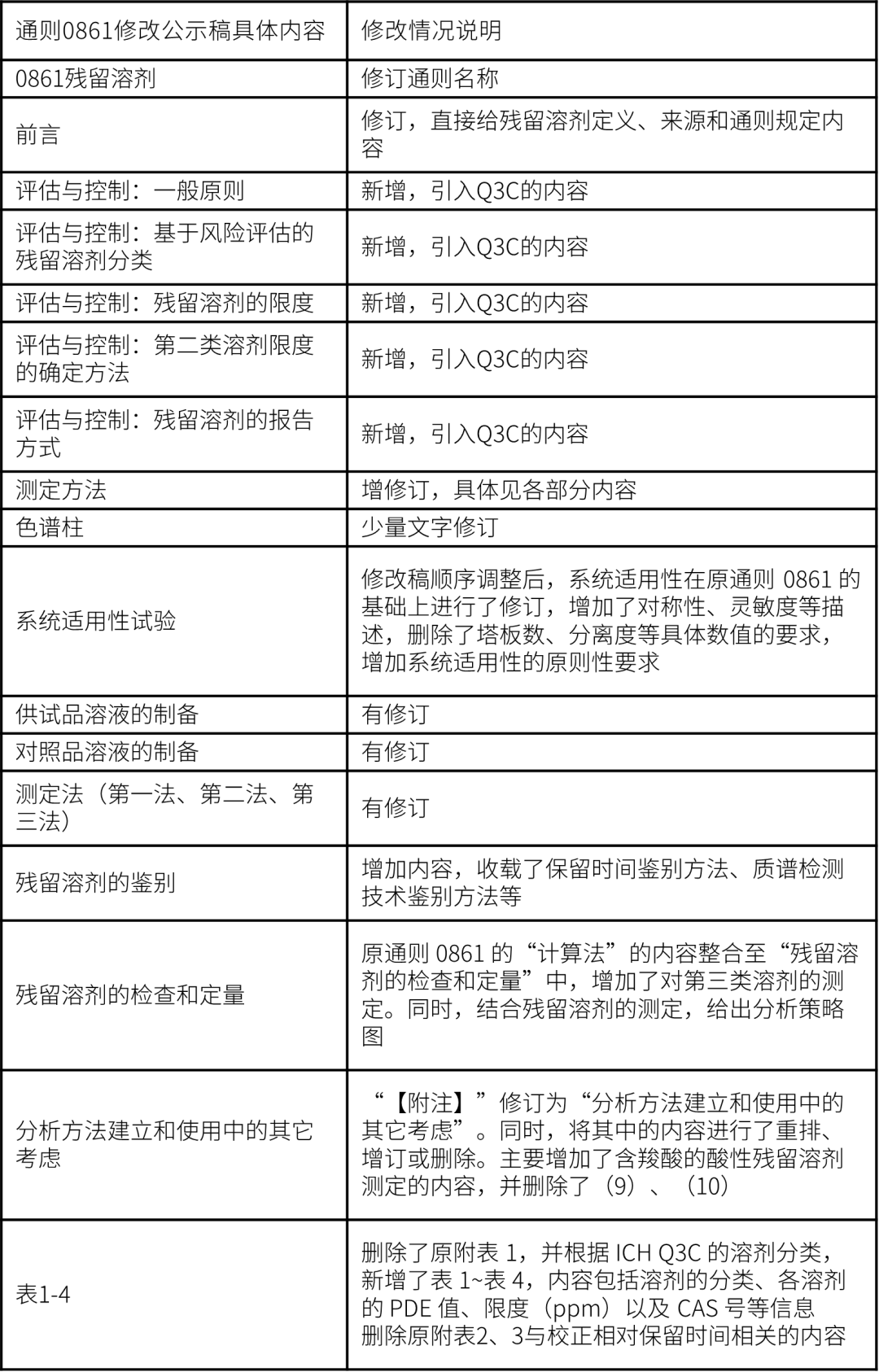
总体来说,除了通则名称修订、引入ICH Q3C评估与控制的核心内容即新增“评估与控制”部分外,公示稿的主要修订内容有:将原通则0861有关测定法内容整合为“测定方法”,删除例如塔板数、分离度等具体数值的要求,增加系统适用性的原则性要求,描述更加严谨,同时还新增了“残留溶剂的鉴别”,对第三类溶剂的测定,结合残留溶剂的测定给出分析策略图等。
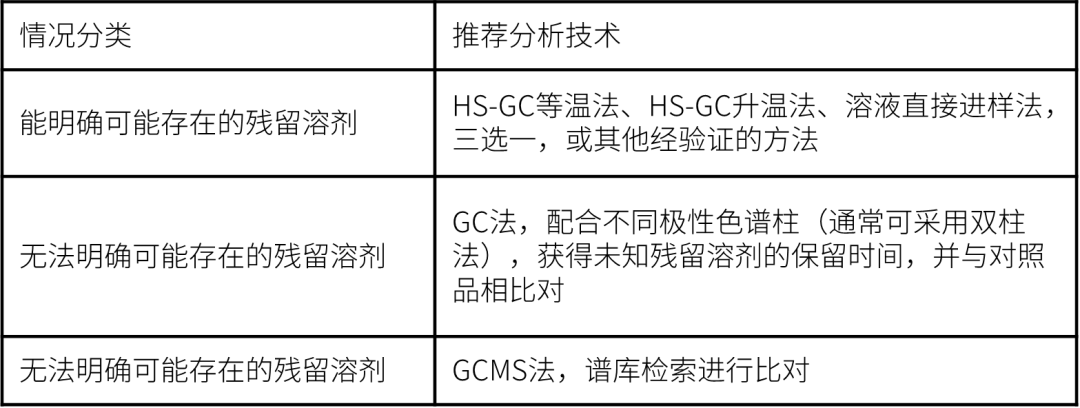
其中,充分理解“分析策略图”非常重要,津津老师也为大家简化整理了分析策略图中所涉及的分析技术:

HS-20NX+气相色谱仪GC-2030
SHIMADZU

HS-20NX+气相色谱质谱联用仪GCMS-QP2020NX
SHIMADZU
虽然在具体测定方法、系统适用性要求、供试品和对照品溶液制备等方面存在差异,但对于残留溶剂,即在原料药、辅料或制剂生产过程中使用或产生的并在实际工艺过程中不能完全除去的有机挥发性化合物,一般推荐方法仍然是经典的气相色谱法。0861通则测定法共3个方法,其中第1法和第2法都是搭配顶空进样器来完成分析。在未知残留溶剂的鉴定方面,质谱检测器是对保留时间定性有力的补充,因此近年来气相色谱质谱联用仪的应用也更为普及。
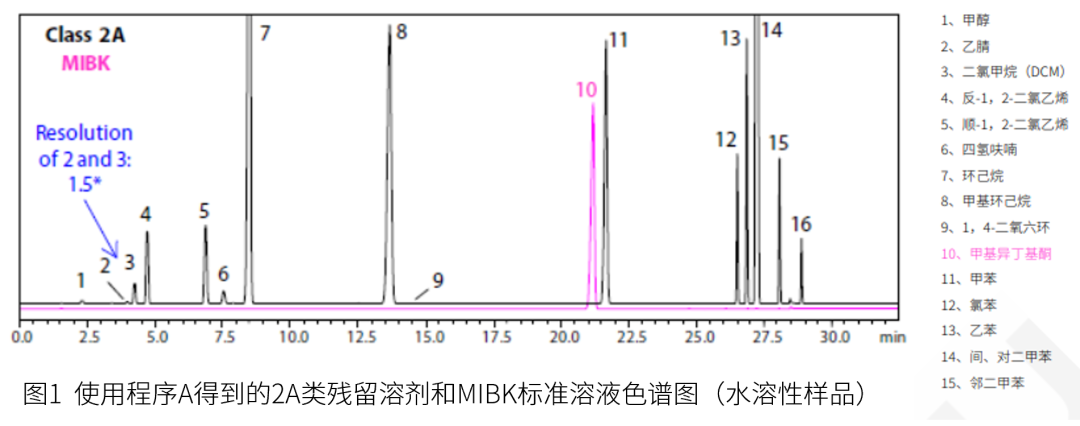
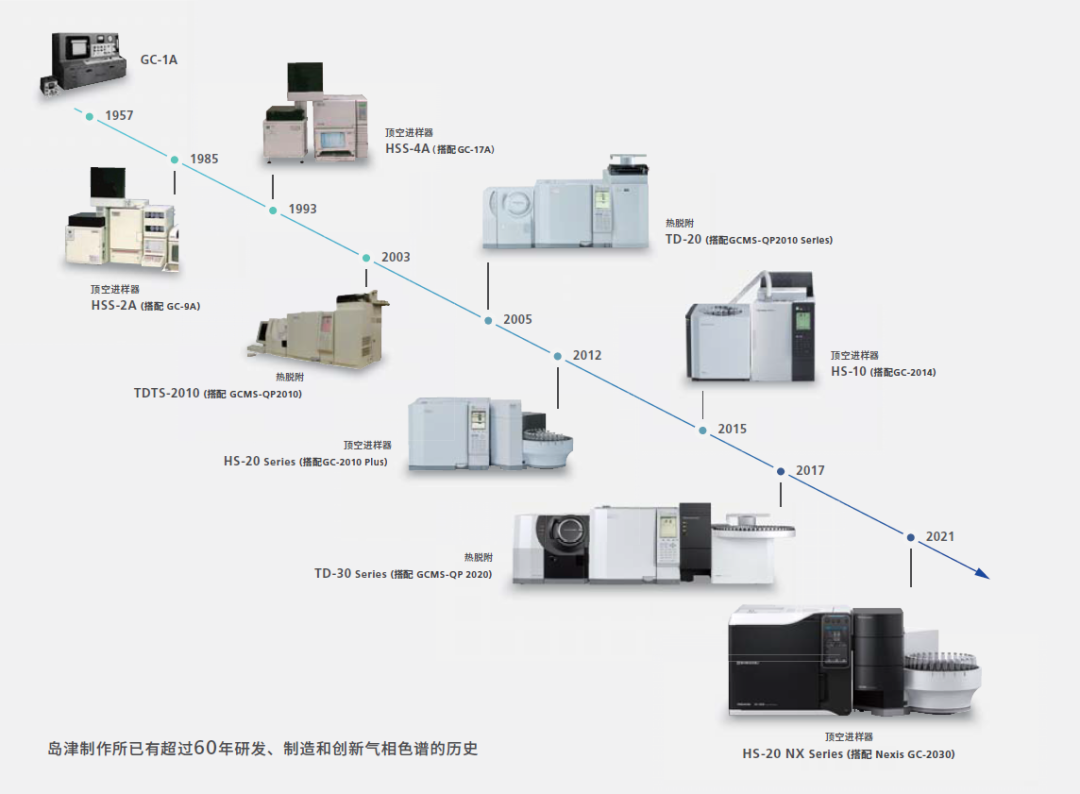
岛津是气相色谱仪的专业供应商,岛津的气相色谱仪已有60多年的发展历程,对于原料药、药用辅料或制剂中的残留溶剂,我们为客户提供完整且严谨的解决方案,涵盖水溶性、非水溶性等各类样品的分析,我们拥有丰富的经验可以与客户分享,包括HS-GC-FID法、HS-GC-MS法,GC-FID法和GC-MS法等,应用方案已覆盖0861修订稿(同ICH Q3C表1-表4)的5种第1类溶剂,31种第2类溶剂,27种第3类溶剂以及9种第4类溶剂的全面分析。

岛津HS-20NX顶空进样
★ 性能智优:隔离流路设计避免了样品在排空管路中的扩散,配合超短惰性流路,残留量降低为原来的1/10,让高沸点、高极性物质分析结果更加可靠
★ 操作智慧:兼容前端气相的ClickTek技术,实现免工具安装色谱柱,配合12位重叠加热位,让分析和维护更加便捷
★ 聚焦智敏:trap模式下可以用电子冷阱实现对宽沸点范围内物质的富集,进一步提升分析的灵敏度,实现超痕量分析
SHIMADZU

更多应用数据可参阅岛津《化学药品中残留溶剂检测应用文集》,更多机型欢迎垂询岛津。复制以下链接前往浏览器打开下载文集:
https://support.shimadzu.com.cn/literature/AP_NOTES/SGCOE-22-08.html
本文内容非商业广告,仅供专业人士参考。


