特色方案|复合膜类药包材中溶剂残留量的测定(GC-MS 法)

复合膜类药包材中
溶剂残留量的测定
SH-PolarWax GC-MS

药品包装材料中的溶剂残留物可能对药品的质量和稳定性产生负面影响。通过测定溶剂残留量,可以确保药品包装材料的质量符合相关的标准和法规要求。此外,准确测定溶剂残留量还有助于确定包装材料的适用性和稳定性,并为药品的质量控制提供基础。
摘要
本文建立了复合膜类药包材中溶剂残留量测定的 GC-MS 方法。参照《药包材溶剂残留量测定法征求意见稿》种第三法中条件并优化,采用色谱柱 SH-PolarWax 对 16 种化合物进行分析,岛津 GCMS-QP2020NX 气相色谱-质谱联用仪进行检测。结果表明,16 种化合物峰型对称,重现性好,满足标准要求。本方法可为药包材中溶剂残留量的测定提供参考。
01
实验部分

1.1 实验仪器及耗材
仪器配置:岛津 GCMS-QP2020 NX 气相色谱-质谱联用仪;HS-20 NX 顶空自动进样器
纯水机:PR-FP-0120α-MT1(+ 60L 水箱 + 取水器)
色谱柱:SH-PolarWax(60 m × 0.25 mm × 0.5 μm;P/N:R227-36248-02);SHIMSEN Disc HPTFE 针式过滤器(P/N:380-00341)
GC-MS 认证样品瓶 LabTotal Vial(P/N:227-34002-01);
SHIMSEN Pipet 移液枪:SHIMSEN Pipet PMII-10(P/N:380-00751-02);
SHIMSEN Pipet PMII-100(P/N:380-00751-04);SHIMSEN Pipet PMII-1000(P/N:380-00751-06)。
1.2 对照品溶液的制备
2000 μg/mL 混合对照品溶液:取 16 种化合物混标母液(2000 μg/mL,溶剂为 DMF)20 μL注入顶空瓶中,立即压盖密闭。
100 μg/mL 混合对照品溶液:取 16 种化合物混标母液(2000 μg/mL,溶剂为 DMF)适量,加 DMF,配成 100 μg/mL 的混合对照品溶液。取 100 μg/mL 混合对照品溶液 20 μL 注入顶空瓶中,立即压盖密闭。
10 μg/mL 混合对照品溶液:取 100 μg/mL 混合对照品溶液适量,加 DMF,配成 10 μg/mL 的混合对照品溶液。取 10 μg/mL 混合对照品溶液 20 μL 注入顶空瓶中,立即压盖密闭。
1.3 供试品的制备
取内表面为 200 cm2 的试样:剪成 1cm×3cm 大小,置顶空瓶中,压盖,密封。
1.4 分析条件
GC 条件
毛细管柱: SH-PolarWax(60 m × 0.25 mm × 0.5 μm;P/N:R227-36248-02)
程序升温:初始温度 65 °C,保持 10 min,以 10°C/min 升温到 150 °C,保持 10 min
载气:He
载气控制模式:恒线速度
流速:1.0 ml/min
进样量:1 μL
进样方式:分流(10:1)
HS 条件
恒温炉温度:100 °C
样品流路温度:150 °C
传输线温度:150 °C
样品瓶恒温时间:50 min
质谱条件
电离模式:电子轰击电离(EI)
离子源温度: 230 °C
接口温度:200 °C
溶剂延迟:2 min
检测器电压:调谐电压+0.1 kV
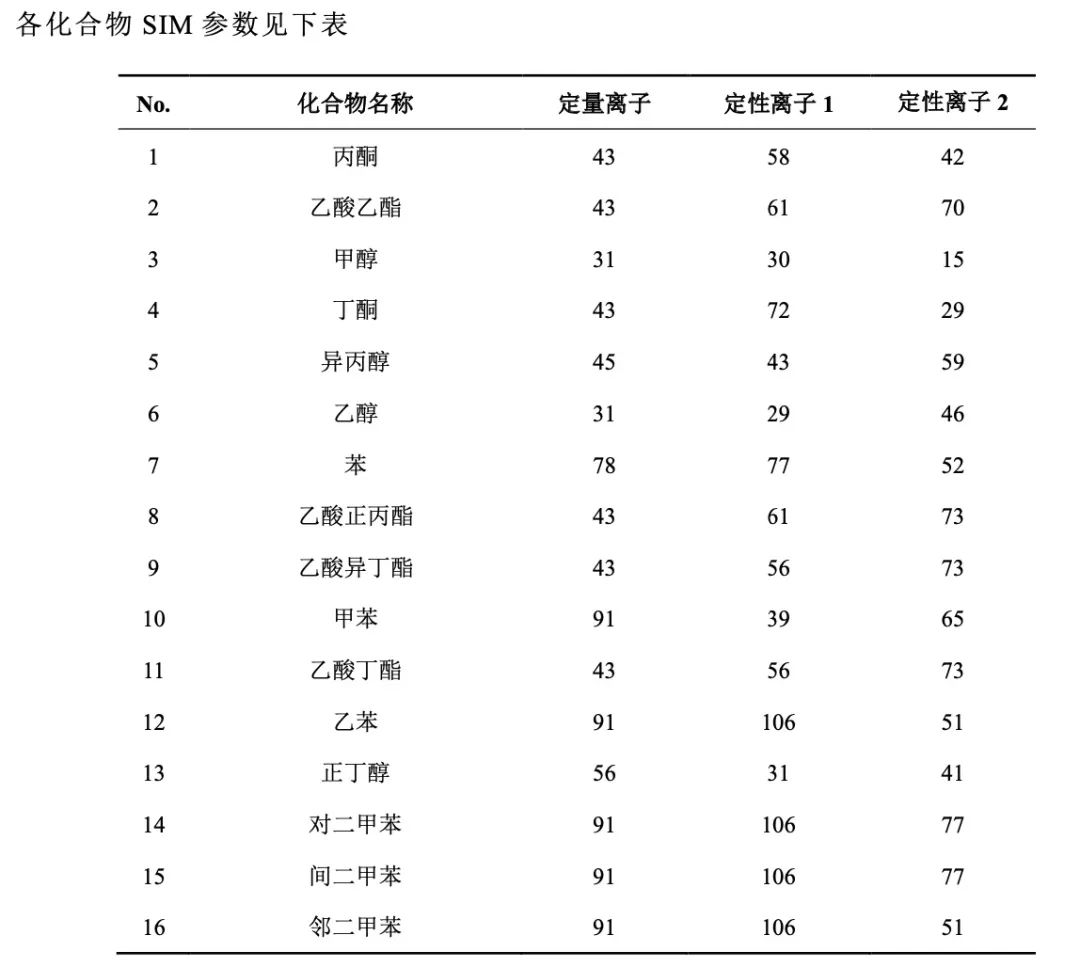
数据采集模式: SIM
02
实验结果
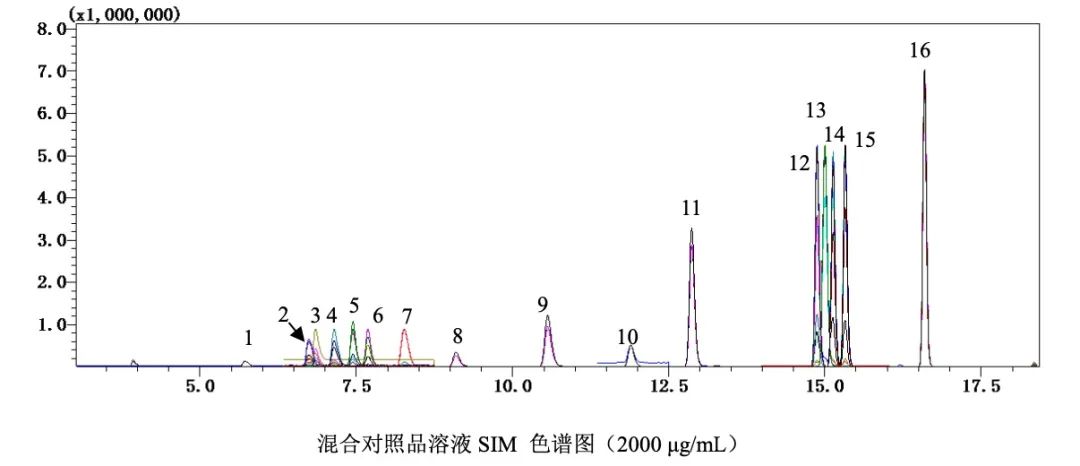
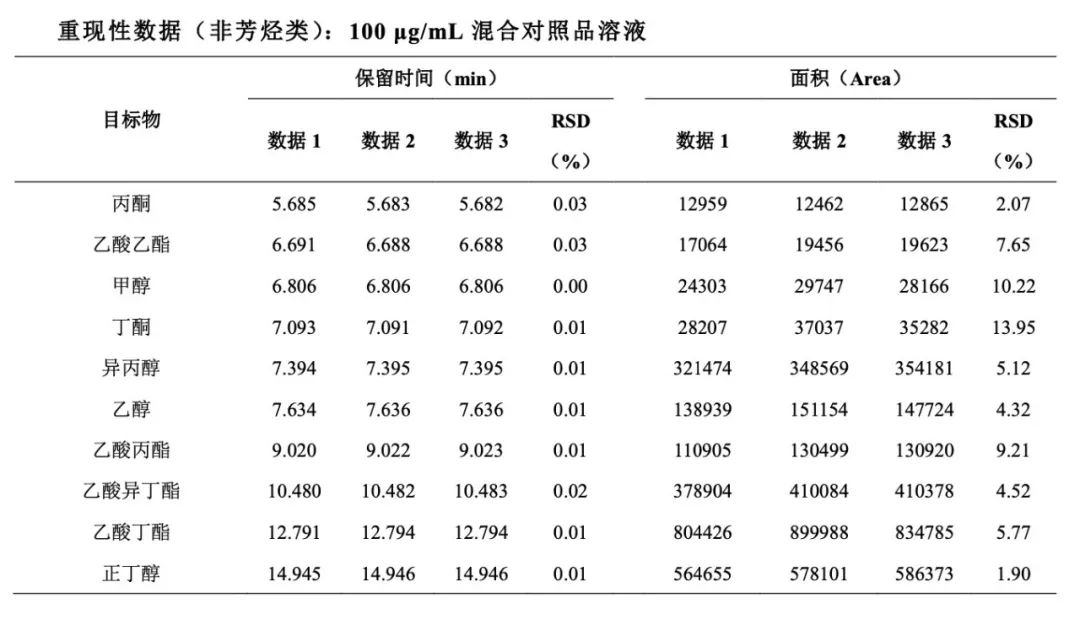
按照上述色谱条件(1.4)进行采集,色谱图如下:

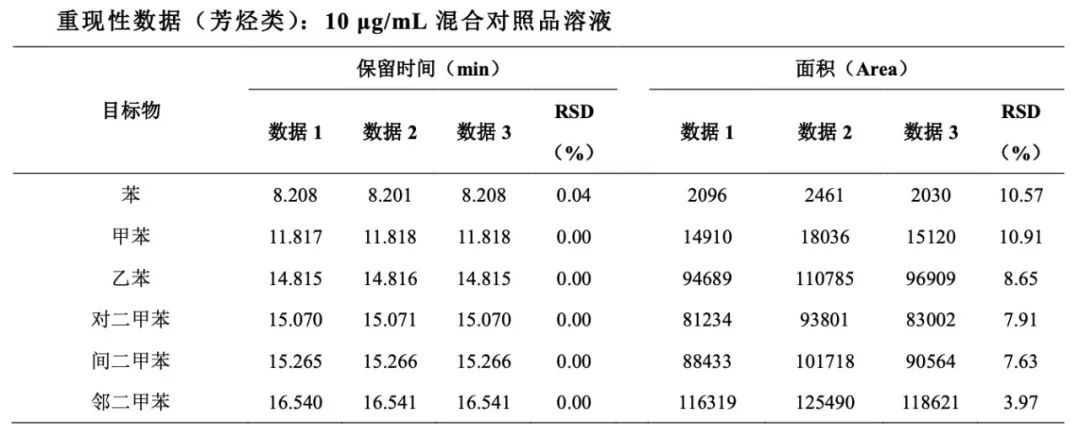
03
结论
本文建立了复合膜类药包材中溶剂残留量测定的GC-MS方法。参照《药包材溶剂残留量测定法征求意见稿》种第三法中条件,采用色谱柱SH-PolarWax 对16种化合物进行分析,岛津GCMS-QP2020 NX气相色谱-质谱联用仪进行检测。结果表明,16种化合物峰形对称,重现性好,满足标准要求。本方法可为药包材中溶剂残留量的测定提供参考。