成像质谱显微镜在中药研究应用专辑-不同生长期药材研究案例盘点


采收药材既要考虑到因品种、产地不同而致采收时日不同,也要考虑到即使同一品种因治疗目的的不同而可能有不同的采收期限。随着现代科学研究的发展,很多药用植物都有了新的适应症,这与药材内有多种有效成分的存在是分不开的,各个成分可能单独或协同作用于治疗目的。如铁皮石斛,含有生物碱、多糖和氨基酸等有效成分,对石斛不同生长期的产量、有效成分含量及功效进行综合分析。铁皮石斛以清音明目为治疗目的,应在第4年采收,以增强免疫为治疗目的,宜在第1或第3年采收。
采收期不仅对药材的外观特征有影响,还直接决定了其内在品质和药用价值。近年来,有中药研究机构使用质谱成像技术开展药材不同生长期研究,岛津技术团队结合与药品检验机构合作案例及文献开展本次案例分享。
岛津中国创新中心与河北省药检院国家药监局中药材质量监测评价重点实验室研究团队合作,采用成像质谱显微镜(iMScope QT)研究了连翘中的主要活性成分的分布,并探讨了成像质谱显微镜用于连翘质量控制的新方法,合作成果在2024年7月发表在《Journal of Mass Spectrometry》杂志上。

连翘(Forsythia suspensa (Thunb.) Vahl)是木樨科连翘属灌木,广泛分布于山西、河南、陕西等地,以野生资源为主,具有显著的抗炎、抗菌、抗氧化和抗病毒活性。本研究子项目之一是采用iMScope QT测定了不同采收期连翘中化学成分的分布,从而了解整个生长期内活性成分变化规律,提出了新的研究思路。


青翘(果实初熟时采收)
老翘(果实熟透时采收)
通过质谱成像分析,在连翘果实中可以检测到多达53种药物活性成分,证明基于大气压MALDI的质谱成像技术是一种评价连翘品质的有效方法。连翘果实包含三个主要部分(果皮(pericarp)、顶部(top)和果核(kernel))。图1显示了15种典型活性成分在青翘全果中的分布。其中,以[M+K]+的形式检测到9个,以[M+Na]+的形式检测到3个,以[M+H]+的形式检测到3个。连翘中钾含量较高,可能高含量的钾促进了MALDI离子源中[M+K]+的生成。

图1 药物活性成分在连翘果实中的分布(曹川,2022)
本研究检测到的26种活性成分根据活性成分变化规律和含量水平可以分为四组,分别命名为G1、G2、G3和G4。图2展示了G1和G2组活性成分随采收时间的变化规律,连翘酯苷A在后期含量显著下降,验证了药典结论。
G1组包括连翘梾木苷、连翘脂苷、金丝桃苷、槲皮素、化合物A、二氢杨梅素和阿魏酸;
G2组包括连翘苷、罗汉松脂苷、毛柳苷和连翘酯苷A;
G3组包括Onjixanthone I、羟基熊果酸、白桦脂酸、木犀草素7-O-(6''-丙二酸单酰葡萄糖苷)、鸢尾苷、汉黄芩苷和连翘梾木苷A;
G4组化合物包括芦丁、连翘环己醇苷A、连翘环己醇苷B、山茱萸苷、五福花苷酸、熊果酸、橙皮苷和木通苯乙醇苷 A。
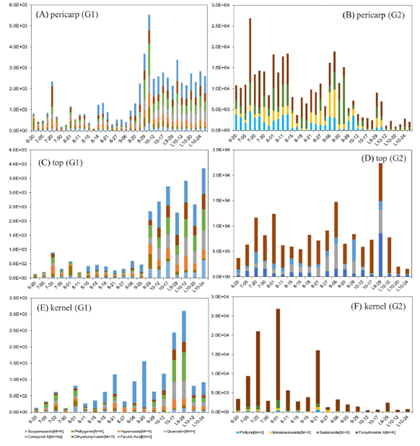
图2 G1和G2组成分的相对含量与采收时间的关系(采样日期含“L”的样品为老翘,曹川2019)
活性成分的含量变化与其生物合成和降解密切相关。图3总结了连翘果实中典型成分的生物合成和降解途径。作为生物合成的最终产物,连翘酯苷A、连翘苷和毛柳苷在青翘中的含量高于老翘中的水平是合理的(图2)。一旦生物合成停止(或者当果实成熟时),糖苷类化合物会发生脱糖基化、脱水和水解反应,这些反应有助于老翘中金丝桃苷和槲皮素的积累(图3(a))以及连翘脂素和阿魏酸(图3(d))的增加。连翘梾木苷A(suspensaside A)和木通苯乙醇苷 A(calceolarioside A)也含有糖苷键,但它们的含量变化不大(G3和G4组)。这可能是因为连翘梾木苷(suspensaside)的降解能补偿它们的损失(图3(c))。山茱萸苷(cornoside)、连翘环己醇苷 A(rengyoside A)和连翘环己醇苷 B(rengyoside B)的含量变化也不显著(G4组)。山茱萸苷的氧化可以补偿毛柳苷(salidroside)的损失。对于连翘环己醇苷 A和连翘环己醇苷 B,也许化合物的稳定性足够高,因此从青翘到老翘它们的含量变化不显著(图3(b))。
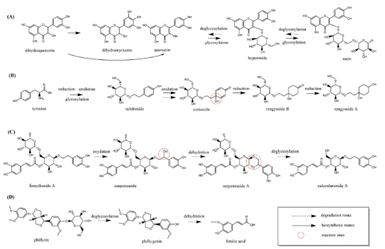
图3 五种成分在连翘果实中的生物合成及降解途径

枸杞子作为我国传统名贵中药材,具有滋肝补肾、益精明目的功效。目前,枸杞子作为中药材和功能食品在全世界广泛使用,也是西北各省的重要经济作物。在枸杞果实成熟过程中,它产生的内源性分子构成了复杂的空间代谢网络,这些内源性代谢物在植物的抗病防御反应及信号传递中发挥着重要作用,更为重要的是它们也是天然药物的重要来源。因此,揭示药用植物不同生长阶段中次生代谢产物的组织分布特征及其累积规律,对其次生代谢产物合成研究以及调控、优化栽培生产技术、培育和保护优良种质资源等方面都有重要意义。
在本研究中,使用质谱成像技术建立了一种简单、可靠的方法直接可视化枸杞果实组织中内源性分子的空间分布特征,为进一步了解枸杞果实生长过程中内源性分子的生理作用提供了一种空间可视化方式,同时突出了质谱成像作为一种可行性工具在药用植物领域的应用潜力。本研究实验思路见图1。
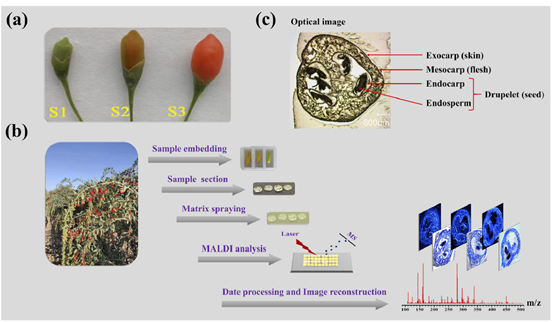
图1 利用质谱成像技术可视化枸杞果实中内源性分子分布
采集花后15d、28d、31d的枸杞果实作为研究样品,分别对应S1期(绿色)、S2期(黄绿色)和S3期(红色)。采用iMScope TRIO 成像质谱显微镜对三个不同生长期的枸杞果实进行了糖(己糖、蔗糖)、柠檬酸、生物碱(甜菜碱、胆碱)及多酚类内源性分子的空间分布分析。如图2所示,胆碱、甜菜碱和柠檬酸在所有生长期均匀分布在整个果实中。己糖分布于内果皮和果肉组织中,而蔗糖位于种子中。
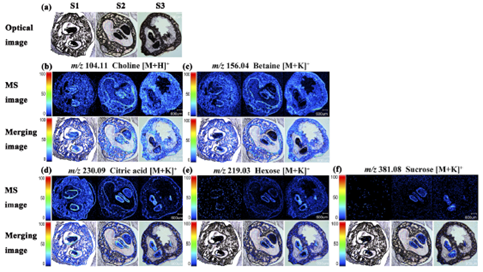
图2 (a) S1 ~ S3时期枸杞果实的光学图像。(b-f)正离子模式:m/z 104.11(胆碱)、156.04(甜菜碱)、230.09(柠檬酸)、219.03(己糖)和381.08(蔗糖)的质谱成像图
随着果实发育,柠檬酸的信号强度在减弱,而胆碱、甜菜碱、己糖和蔗糖的信号强度在增加。此外,如图3所示,随着果实成熟,三种酚酸和四种黄酮类化合物在外果皮中积累。有报道称,酚类化合物在植物抵御病原菌侵袭和紫外线照射方面发挥着重要的保护作用。这表明它们可能在枸杞果实生长过程中发挥了某种非生物和生物胁迫的保护作用,具体作用机制需要进一步研究。

图3 (a) S1 ~ S3时期枸杞果实的光学图像。(b-h)负离子模式:m/z 163.04(对香豆酸)、179.03(咖啡酸)、285.04(山奈酚)、301.03(槲皮素)、315.05(异鼠李素)、353.09(绿原酸)和463.09(异槲皮素)的质谱成像图
本研究结果有助于更好的了解枸杞子不同成熟期生物活性物质的分布,为枸杞子成分识别、质量评价、高值化利用等提供参考。
以上内容是对研究文献的概述,如需了解详细内容,可根据以下文献目录搜寻全文。
参考文献
【1】Liu Y ,Wang C ,Chen Z , et al.Distribution of active ingredients and quality control of Forsythia suspensa with AP-MALDI mass spectrometry imaging.[J].Journal of mass spectrometry : JMS,2024,59(8):e5073.
【2】]Hua W Z ,Da Y Z ,Ping Y S .Visualizing the spatial distribution of endogenous molecules in wolfberry fruit at different development stages by matrix-assisted laser desorption/ionization mass spectrometry imaging[J].Talanta,2021,234122687-.

iMScope成像质谱显微镜是用于质谱成像分析的整合型仪器,前端搭载高分辨光学显微镜及大气压基质辅助激光解吸电离源(Atmospheric Pressure -MALDI,AP-MALDI),后端配置四极杆-飞行时间质谱仪(Q-TOF)iMScope既可以对样品进行形态学上的细微观察,又可以对特定的分子进行鉴定以及高分辨的可视化分布分析。
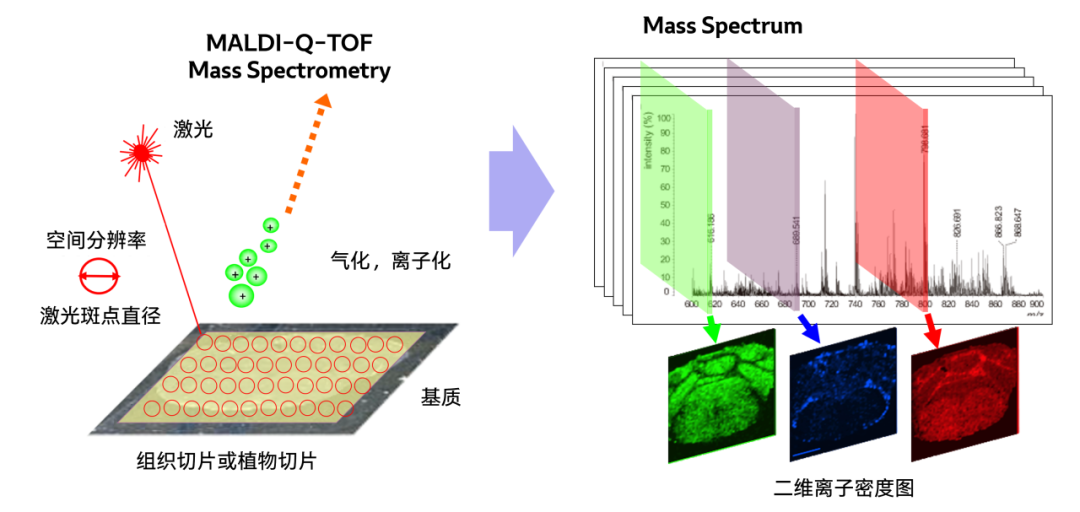
质谱成像原理示意图
岛津成像质谱显微镜iMSCope QT 的特点
• 5 μm高空间分辨率
• 显微镜观察和质谱成像分析的融合
• 高速分析,激光器扫描频率高至 20 kHz,最快成像速度50 像素/秒
• 兼容LC-QTOF系统,一台仪器同时完成定性、定量及定位分析
• 常压MALDI,可以分析具有一定挥发性的样品,如多环芳烃和姜黄素
• 配备完整的前处理基质涂敷设备(基质升华仪iMLayer 与全自动喷雾仪iMLayer AERO)
• 简便、专业的成像分析软件IMAGEREVEAL MS
撰稿人:丰伟刚

本文内容非商业广告,仅供专业人士参考。






